Fierbinte (reprezentat prin litera Q) este energie transferată de la un sistem la altul (sau de la un sistem la împrejurimile sale) în general datorită unei diferențe de temperatură între ele. Căldura pe care un sistem termodinamic o absoarbe sau o eliberează depinde în mod normal de tipul de transformare pe care a suferit-o sistemul.
Două sau mai multe corpuri în contact care se află la temperaturi diferite ating, după un timp, echilibrul termic (aceeași temperatură). Acest fapt este cunoscut sub numele de Principiul zero al termodinamicii, și este ilustrat în figura următoare.
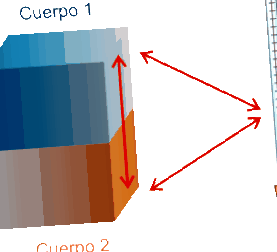 |
Un aspect al căldurii care ar trebui evidențiat este că corpurile nu depozitează căldură ci energie internă. Prin urmare, căldura este transferul unei părți din energia internă menționată de la un sistem la altul, cu condiția ca ambele să fie la temperaturi diferite. Unitățile sale din sistemul internațional sunt joule (J)
Expresia care leagă cantitatea de căldură pe care o masă m dintr-o anumită substanță o schimbă cu modificarea temperaturii Δt pe care o experimentează este:
unde c este căldura specifică a substanței.
Căldura specifică (sau capacitate termică specifică) este energia necesară pentru a crește temperatura de 1 kg de masă cu 1 grad. Unitățile sale din sistemul internațional sunt J/kg K.
În general, căldura specifică a unei substanțe depinde de temperatură. Cu toate acestea, deoarece această dependență nu este foarte mare, este tratată de obicei ca o constantă. Acest tabel arată căldura specifică a diferitelor elemente ale tabelului periodic și în acest tabel căldura specifică a diferitelor substanțe.
Când se lucrează cu gaze, este destul de obișnuit să se exprime cantitatea de substanță în termeni de număr de moli n. În acest caz, se numește căldura specifică capacitatea de căldură molară C. Căldura schimbată este apoi dată de:
În sistemul internațional, unitățile de capacitate termică molară sunt J/molK.
- Criteriul semnelor: De-a lungul acestor pagini, căldura absorbită de un corp va fi pozitivă, iar căldura eliberată negativă.
Capacitatea termică a unui gaz ideal
Pentru un gaz ideal, sunt definite două capacități de căldură molară: a volum constant (CV) și presiune constantă (Cp).
- CV: este cantitatea de căldură necesară pentru a furniza un mol de gaz ideal pentru a-și crește temperatura cu un grad prin intermediul unei transformări izocorale.
- Cp: este cantitatea de căldură necesară pentru a furniza un mol de gaz ideal pentru a-și crește temperatura cu un grad printr-o transformare izubară.
Valoarea ambelor capacități de căldură poate fi determinată cu ajutorul teoriei cinetice a gazelor ideale. Valorile respective pentru gazele monatumice și diatomice se găsesc în tabelul următor:
unde R este constanta universală a gazului ideal, R = 8,31 J/mol K.
Căldura latentă a unei schimbări de fază
Când un schimbarea fazei, substanța trebuie să absoarbă sau să renunțe la o anumită cantitate de căldură pentru ca aceasta să aibă loc. Această căldură va fi pozitivă (absorbită) atunci când schimbarea fazei are loc de la stânga la dreapta în figură și negativă (cedată) atunci când tranziția de fază are loc de la dreapta la stânga.
Căldura absorbită sau transferată într-o schimbare de fază nu se traduce printr-o modificare a temperaturii, deoarece energia furnizată sau extrasă din substanță este utilizată pentru a schimba starea de agregare a materiei. Această căldură se numește căldură latentă.
Latent în latină înseamnă ascuns și se numește așa deoarece, deoarece temperatura nu s-a schimbat în timpul schimbării stării, în ciuda adăugării căldurii, a rămas ascunsă fără a fi tradusă într-o schimbare de temperatură.
Căldura latentă (L) sau căldura de schimbare a stării, este energia absorbită sau transferată pe unitatea de masă a substanței la schimbarea stării. De la solid la lichid, această căldură se numește căldură fuziune latentă, de la lichid la vapori căldură latentă de vaporizare și de la solid la abur căldură latentă de sublimare.
Căldura latentă pentru procesele inverse (reprezentate în albastru în figura precedentă) au aceeași valoare în valoare absolută, dar vor fi negative deoarece în acest caz este o căldură transferată.
În sistemul internațional, căldura latentă este măsurată în J/kg.
Cantitatea de căldură absorbită sau dată de o cantitate m de substanță pentru a schimba faza este dată de:
Această căldură va fi pozitivă sau negativă în funcție de schimbarea de fază care a avut loc.
Pagină realizată de Teresa Martn Blas și Ana Serrano Fernbndez - Universitatea Politehnică din Madrid (UPM) - Spania.
- Primul principiu al termodinamicii
- La jumătate de secol de la primul mers spațial El Diario Vasco
- Baschetul clubului leton nu trebuie subestimat! Jānis Gailītis așteaptă primul derby al
- Pentru gestionarea cronică a supraponderabilității și obezității, Novo Nordisk lansează primul tratament injectabil
- Medicii stomatologi recomandă controale orale regulate la copii după primul dinte
