Rev Méd Chile 2007; 135: 631-635
CAZURI CLINICE
Sindromul deficitului de tip 1 al transportorului de glucoză (SDGLUT-1) tratat cu o dietă ketogenică. Caz clinic
Tipul de transpunere a glucozei 7 sindromul de deficiență (GLUT-1 SD) tratat cu dietă ketogenică. Raportul unui caz
Verónica Cornejo E 1a, Juan Francisco Cabello A 1, Marta Colombo C 2, Erna Raimann B 1 .
1 Laborator de boli metabolice, Institutul de nutriție și tehnologie alimentară (INTA), Universitatea din Chile, 2 Laborator de boli metabolice, Spitalul Van Burén, Valparaíso.
un nutriționist, masterat în nutriție umană
(Cuvinte cheie: Boli ale creierului, metabolice, înnăscute; Transportor glucoză tip 1; Convulsii)
ȘI În 1991, De Vivo a descris sindromul deficienței transportorului de glucoză cerebrală tip 1 (SDGLUT-1) (OMIM 606777), la doi pacienți care au prezentat encefalopatie epileptică care a evoluat cu dezvoltare psihomotorie întârziată, stop de creștere craniană, microcefalie, incoordonare și spasticitate . În plus, a detectat că a existat o scădere a nivelului de glucoză și lactat în lichidul cefalorahidian (LCR), dar nu a găsit hipoglicemie 1 .
SDGLUT-1 are moștenire autosomală dominantă 2. Transportorul Glut-1 este o glicoproteină formată din 492 aminoacizi, responsabilă de transportul glucozei peste bariera hematoencefalică, care se exprimă în celulele endoteliale vasculare, astrocite și neuroni. Gena a fost codificată pe brațul scurt al cromozomului 1 (p34.2) și este compusă din 10 exoni și 9 introni. Până în prezent, au fost descrise mai mult de 30 de mutații. Concentrațiile Glutl și Glut3 s-au dovedit a fi scăzute la naștere și se normalizează la înțărcare, o perioadă corespunzătoare creșterii și maturării crescute. Unii autori au arătat că această glicoproteină este inhibată de fenobarbital 3 .
Istoricul pre și perinatal al unui copil afectat de această patologie este aparent normal până la vârsta de 2 luni, când apar episoade de apnee și mișcări oculare de tip opsoclonus, care pot preceda convulsiile epileptice. Convulsiile din copilărie sunt fragmentate clinic, EEG prezintă descărcări multifocale și au fost descrise tipuri de tonice generalizate, mioclon, absență atipică, atonică și neclasificată. Frecvența poate fi zilnică, ocazională sau fără convulsii 4. Aceste crize nu răspund la anticonvulsivante. Pot fi de asemenea detectate evenimente paroxistice neepileptice, cum ar fi ataxia intermitentă, confuzie mentală, letargie, somnolență, hemipareză, mișcări anormale, paralizie, tulburări de somn, microcefalie sau decelerarea creșterii craniene 5. .
La testele de laborator, se observă hipogliconie persistentă (sub 40 mg/dl), lactatul din LCR poate fi sau nu scăzut (6 .
Tratamentul se bazează pe o dietă ketogenică, care va furniza energia necesară creierului prin corpuri cetonice. Datorită restricției mari a alimentelor naturale bogate în carbohidrați, care la rândul lor sunt o sursă de nutrienți esențiali, dieta trebuie completată permanent cu minerale, vitamine liposolubile și solubile în apă, L-carnitină și acid lipoic, în funcție de vârstă și sex 7-10 .
Descriem clinica, biochimia, studiul molecular și urmărirea pe termen lung a primului caz de SDGLUT-1 diagnosticat în Chile.
CAZ CLINIC
Pacient de sex feminin, părinți non-consanguini, fără antecedente perinatale relevante; greutatea la naștere 3-450 g, înălțimea 49,5 cm și circumferința craniului 35,2 cm. Apgar 9, la 5 min.
La vârsta de o lună și jumătate, a prezentat crize tonice generalizate ale tonicului, care durează câteva secunde, evoluând cu 20 de mioclonuri pe zi, adăugând spasme de flexie. A primit tratament farmacologic cu acid valproic, fenobarbital și carbamazepină, fără răspuns clinic, declanșând o reacție adversă la acidul valproic cu hiperamonemie simptomatică.
La vârsta de 3 luni și jumătate, au fost efectuate teste pentru a exclude o boală metabolică, constatându-se o lactacidemie de 26,5 mg/dl (VN: 5-15), o scădere a lactatului LCR de 5,6 mg/dl (VN: 10,8 -18,9 mg/dl). Acidul piruvic în plasmă a crescut (1,4 mg/dl) (VN: 0,3-0,9), dar în LCR a fost normal (0,43 mg/dl) (VN: 0,5-1,7), iar amoniacul a fost de 85 µg/dl (35-100 pg/dl). Cuantificarea aminoacizilor din ser, acilcarninele din sângele integral, acizii organici din urină și carnitina din ser au fost normale.
La 5 luni, electroencefalograma (EEG) a detectat activitate teta-delta polimorfă continuă, considerată anormală pentru vârstă, iar imagistica prin rezonanță magnetică a arătat atrofie frontală cu o creștere a spațiilor subarahnoidiene. A evoluat cu o întârziere în dezvoltarea psihomotorie și decelerarea creșterii craniene, a ataxiei trunchiului și a sindromului piramidal bilateral.
La 7 luni a fost internat la Boston Children's Hospital, din Statele Unite ale Americii, unde s-a constatat o scădere a glucozei LCR de 26 mg/dl și a normoglicemiei (84 mg/dl), obținând un raport între ambii parametri de 0, 31 (valoare normală peste 0,65 + 0,01), în concordanță cu hipoglicorhachia, sugerând un SDGLUT-1.
S-a dovedit că proteina Glut-1 din eritrocit este identică cu proteina Glut-1 a celulelor endoteliale ale capilarelor creierului, atât în răspuns imunitar, cât și chimic. Din acest motiv, transportul glucozei în eritrocit este comparabil cu transportul glucozei peste bariera hematoencefalică. Având în vedere această constatare, a fost dezvoltată tehnica 3-O-metil D glucoză, care determină absorbția glucozei de către eritrocit, permițând extrapolarea cu transportul glucozei în bariera hematoencefalică 11. În cazul nostru, s-a aplicat această tehnică, obținându-se o absorbție de glucoză de 44% (VN 80% -100%), confirmând un SDGLUT-1.
În studiul molecular, s-au utilizat reacția în lanț a polimerazei (PCR) și analiza polimorfismelor de fragment de restricție (RFLP) 3,6, determinând mutația grupului de deleție 969, C971T, situat în exonul 6, al genei Glut. 1 (Figura 1) (Studiu molecular realizat de Dr. D. De Vivo).
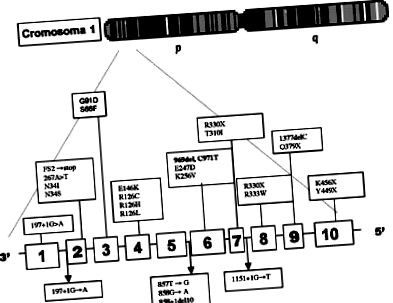 |
| Figura 1. Mutații identificate care cauzează SDGLUTl. Barele numerotate reprezintă cei 10 exoni și 9 introni care alcătuiesc gena Glut-1, situată pe brațul scurt al cromozomului 1 (1p34.2). Mutația |
Tomografia computerizată cu emisie de fotoni unici (SPECT) a arătat hipometabolism bilateral temporal, parietal stâng și talamic.
Dieta ketogenică a fost inițiată imediat, oferind 90 de calorii pe kilogram de greutate, cu 85% lipide, 9% proteine și 6% carbohidrați, cu un raport 3: 1 între lipide și proteine plus carbohidrați, pe baza protocolului utilizat în INTA, din Universitatea din Chile 9,10. Dieta interzice alimentele cu zaharoză, sorbitol, fructoză și lactoză este restricționat, motiv pentru care a fost necesar să se completeze cu calciu (450 mg/zi), zinc (5 mg/zi), vitamine, în special vitamina C (1 g/zi) pentru a preveni oxidarea celulară, L-carnitină (50 mg/kg/zi) și acid lipoic (200 mg/zi).
După 7 zile de la începerea dietei ketogenice, convulsiile au dispărut și, în comun, a început scăderea anticonvulsivantelor.
În prezent, în vârstă de 6 ani, el menține dieta ketogenică cu 83% lipide (27% dintre acestea corespund trigliceridelor cu lanț mediu) și 17% proteine plus carbohidrați (raport de 2,5: 1). Suplimentarea cu nutrienți este la fel ca la început și au fost adaptate în funcție de vârstă și starea nutrițională.
Glicemia rămâne la valori de 80 până la 90 mg/dl, colesterolul total la 187 mg/dl, HDL la 55 mg/dl și LDL la 121 mg/dl. Calciuria, creatininuria, profilul biochimic, gazele venoase și electroliții plasmatici se încadrează în limite normale. Acidul beta hidroxibutirat în post este de 2,5 µM/1 și postprandial este de 5,0 µM/L, luând în considerare cetogeneza atunci când această valoare este mai mare de 2,0 µM/1.
În examinarea neurologică, comportamentul hiperactiv se remarcă în examinarea sa mentală. În nervii cranieni, el prezintă disartrie și hipomimie facială. Examenul motor prezintă scăderea tonusului trunchiului și membrelor, fără compromiterea forței sau a trofismului muscular. La examinarea cerebeloasă, există un tremur fin de intenție, prezența sincineziei, dismetriei și disdiadochokinezei discrete. Mersul este instabil și se caracterizează printr-o creștere a bazei de sprijin, fără lateralizare.
Coeficientul său de inteligență (IQ), evaluat prin testul de inteligență Wechs-ler pentru preșcolari (WISP) 12, a obținut un IQ total de 103 puncte, limita superioară a intervalului mediu normal, corectat în conformitate cu standardele nord-americane. Cu toate acestea, prezintă o discrepanță semnificativă între scara verbală și manuală, în detrimentul acesteia din urmă (IQ verbal: 119, IQ normal ridicat și manual: 85, normal lent), ceea ce se traduce prin dificultăți specifice în organizarea vizuo-spațială și vizomotorie.
Starea nutrițională este normală: indice de masă corporală de 15,8 kg/m 2 (VN între 15 și 18 kg/m 2) 13, cu greutate (21 kg) pentru vârstă și înălțime (1,16 m) pentru vârstă, ambii parametri la nivelul Percentila 75 a tabelului de referință (Centrul Național pentru Statistici de Sănătate) 14 .
Din 1991 până astăzi, aproximativ 100 de cazuri au fost diagnosticate în lume, toate prin manifestări clinice 15 .
Majoritatea cazurilor descrise în literatură au avut un istoric normal pre și perinatal, iar prima manifestare clinică a constituit convulsii în primele 4 luni de vârstă, fără răspuns la tratamentul anticonvulsivant. A existat, de asemenea, o scădere a glucozei și lactatului în lichidul cefalorahidian, egală cu ceea ce a fost detectat în cazul nostru. Cu toate acestea, diagnosticul diferențial a fost extins la alte simptome clinice, deoarece a fost descris la copiii care au avut doar mișcări anormale ale ochilor și la care a fost suspectat inițial un neuroblastom ocult. Prin urmare, se sugerează ca la orice copil cu un tablou clinic sugestiv și cu glicemie normală, valoarea glucozei LCR să fie evaluată pentru a exclude GLUT-1 3 .
Un alt punct important este răspunsul pozitiv la dieta ketogenică, care suprimă convulsiile. Corpurile cetonice intră în creier prin intermediul transportorului monotriccarboxilic utilizat de acizii grași cu lanț mediu, care sunt metabolizați exclusiv în matricea mitocondrială în acetil-CoA, transformând acest substrat în singurul combustibil cerebral. În cazul clinic prezentat, dieta ketogenică a început la vârsta de 7 luni, iar convulsiile s-au oprit imediat. Până în prezent, el menține această dietă și nu a mai manifestat convulsii 8 .
Dieta ketogenică este frecvent utilizată în epilepsia refractară, arătând că acționează ca un anticonvulsivant natural, asociind acest efect cu prezența acidului beta-hidroxibutirat. Mai multe studii au arătat că utilizarea sa pe termen lung nu provoacă tulburări de creștere în greutate 16,19. În cazul nostru, dieta ketogenică are un raport între lipide și proteine plus carbohidrați de 3: 1, a fost adaptată cerințelor nutriționale în funcție de vârstă și greutate, subliniind satisfacerea nevoilor de vitamine și minerale. După aproape 6 ani de urmărire, pacientul are o creștere normală, observând greutatea și înălțimea în percentila 75, LMC de 15,8 kg/m2, în intervalul normal pentru vârsta ei.
Toate cazurile descrise au o anumită afectare cognitivă, care variază de la dizabilități de învățare până la retard mental sever. Mai mult, s-au observat modificări ale limbajului, descriind disartria, cu alterarea limbajului expresiv și receptiv 1 5. Cazul nostru are o dezvoltare cognitivă normală, cu un IQ total de 103 și un IQ verbal de 119, acesta din urmă clasificat în intervalul normal ridicat, care care diferă de ceea ce se găsește în literatură. Acest lucru ar putea fi atribuit a două motive: unul dintre ei este vârsta diagnosticului, deoarece majoritatea pacienților descriși au fost depistați târziu. Cealaltă este că unele mutații ale absenței sau tipului de ștergere au fost asociate cu o formă clinică moderată. Corelația genotip/fenotip propusă este o ipoteză care necesită confirmarea unui număr mai mare de cazuri. Mai mult, mutația găsită în cazul nostru nu a fost descrisă într-o altă familie 3,20 .
REFERINȚE
1. De Vivo D, Trifiletti R, Jacobson R, Roñen G, Behmand R, Heik S. Transportul deficient al glucozei în bamerul sânge-creier ca cauză a hipoglicorhahiei persistente, convulsiilor și întârzierii dezvoltării. N Engl J Med. 1991; 325: 703-9. [Link-uri]
2. Wang D, Brockmann K, Korenke CG, Von Moers A, Ho YY, Pascual JM și colab. Sindromul de deficiență de glut-1: transmiterea autozomală a dominației mutației R126H missense. Ann Neurol. 2001; 50: S124. [Link-uri]
3. Wang D, Pascual J, Yang H, Engelstad K, Jhung S, Peng Sun R, De Vivo D. Sindromul deficitului de glut-1: aspecte clinice, genetice și terapeutice. Ann Neurol. 2005; 57: 111-18. [Link-uri]
4. Von Moers A, Brockmann K, Wang D, Korenke CG, Huppke P, De Vivo DC, Hanefeld F. EEG caracteristici ale sindromului de deficiență de glut-1. Epilepsie. 2002; 43: 941-5. [Link-uri]
5. Pascual J, Wang D, Lecumberri B, Yang H, Mao X, Yang R, De Vivo D. Deficitul GLUT1 și alte boli ale transportorului de glucoză. Eur J Endocrinol. 2004; 150: 627-33. [Link-uri]
6. Pascual J, Van Heerttum R, Wang D, Engelstad K, De Vivo D. Imaginarea amprentei metabolice a deficitului de Glutl pe creier. Ann Neurol. 2002; 52: 458-64. [Link-uri]
7. Acosta P. Defect proteic de transport al glucozei, deficit de complex piruvat-dehidrogenază și convulsii intratabile. În: Acosta P, Yannicelli S. eds. Protocoale de sprijin nutrițional: Editorial Abbott Laboratories, 2001; 279-95. [Link-uri]
8. Klepper J, Diefenbach S, Kohlschütter A, Voit T. Efectele dietei ketogenice în sindromul de deficit al transportorului de glucoză 1. Prostaglan-dins Acizi grași esențiali Leukot. 2004; 70: 321-7. [Link-uri]
9. Dogwood V. Dieta ketogenică în tratamentul epilepsiei refractare. Rev. ChilNutr. 2000; 27: 326-31. [Link-uri]
10. Dogwood V. Dieta ketogenică în pediatrie. În: Sanjurjo P, Baldellou A, eds. Diagnosticul și tratamentul bolilor metabolice ereditare: Editorial Ergon SA, Madrid, Spania, 2001; 111-120. [Link-uri]
11. Klepper J, Garcia Alvarez M, O'Driscoll K, Parides M, Wang D, Yuan HO Y, De Vivo DC. Eritrocitul 3-0. test de absorbție a glucozei metil-D pentru diagnosticarea sindromului glucozei-transport-proteine. J Clin Lab Anal. 1999; 13: 116-21. [Link-uri]
12. Wechsler D. Manual pentru scala de informații Wechsler pentru copii revizuită. San Antonio Texas: Editorial The Psychological Corporation, Harcourt Brace Jovanovich, Inc. 1974. [Legături]
13. Kuczmarski R, Ogden C, Grummer-Strawn L. Diagrame de creștere CDC: Statele Unite. Date avansate din statistici vitale și de sănătate;Nr. 314. Hyattsville, Maryland: Editorial Centrul Național pentru Statistici de Sănătate 2000. [Legături]
14. Villalobos N, Vergara A, Jara C, Orellana N, Maggi A, Torres M, González I. Managementul ambulatoriu al malnutriției din cauza deficitului și excesului la copiii cu vârsta sub 6 ani. Ministerul Sănătății, Guvernul Chile 2005: 7-14. [Link-uri]
15. Gordon N, Newton R. Deficiență de transportor de glucoză tip 1 (GLUT-1). Brain Dev. 2003; 27: 477-80. [Link-uri]
16. Bailey E, Pfeifer H, Thiele E. Utilizarea dietei în tratamentul epilepsiei. Epilepsie și comportament. 2005; 6: 4-8. [Link-uri]
17. Vamecq J, Vallée L, Lesage F, Gressens P, Stables J. Dieta cetogenică populară antiepileptică: răsuciri emergente într-o poveste antică. Neurobiol Prog. 2005; 75: 1-28. [Link-uri]
18. Couch S, Schwarzman F, Carroll J, Koenigsberger D, Nordli D, Deckelbaum R și colab. Creșterea și rezultatele nutriționale ale copiilor tratați cu dieta ketogenică. J Am Diet Conf. Univ. 1999; 99: 1573-5. [Link-uri]
19. Liu Y, Williams S, Basualdo-Hammond C, Stephens D, Curtis R. Un studiu prospectiv: creșterea și starea nutrițională a copiilor tratați cu dieta ketogenică. J Am Diet Conf. Univ. 2003; 103: 707-12. [Link-uri]
20. Wang D, Kranz-Eble P, De Vivo DC. Analiza mutațională a GLUT1 (SLC2A1) în sindromul de deficit de Glut-1. Hum mutat. 2000; 16: 224-31. [Link-uri]
Mulțumiri
Spitalului pentru copii din Boston, în special dr. Darryl De Vivo, care a efectuat studiul molecular al cazului.
Primit pe 9 mai 2005- Acceptat pe 28 august 2006.
Corespondență cu: Prof. Verónica Cornejo E. INTA, Universitatea din Chile. Caseta 13811, Santiago, Chile. Fax: 56-2-2941254. E-mail: [email protected]
Tot conținutul acestei reviste, cu excepția cazului în care este identificat, se află sub o licență Creative Commons
Bernarda Morín 488, Providencia,
Caseta 168, Mail 55
Santiago, Chile
Tel.: (56-2) 2753 5520
- Unul din trei spanioli cu obezitate a încercat un fel de dietă miraculoasă
- V Prezentarea VI #JornadasDSP Dieta ketogenică, prieten sau dușman
- Keto Chives Souffle - Ketotrace Ketogenic Diet
- Ce alimente trebuie evitate în dieta ketogenică Dieta Keto
- Ce să mănânci în funcție de dieta grupei sanguine; Tannos; Chavez
