Amparo Tolosa, Știri despre genetică medicală
Imagine: Petr Kratochvil [CC0], prin Wikimedia Commons Numărul tot mai mare de persoane afectate (peste 600 de milioane în întreaga lume), precum și influența sa asupra diferitelor patologii umane, cum ar fi bolile cardiovasculare, diabetul de tip 2, unele tulburări ale sistemului musculo-scheletic și anumite tipuri de cancer au făcut din obezitate una dintre principalele probleme de sănătate la nivel mondial.
Definită ca o acumulare excesivă de grăsime în organism, dăunătoare sănătății, obezitatea este adesea considerată ca un dezechilibru energetic între cantitatea de calorii consumate și cele consumate. Astfel, alimentația și activitatea fizică joacă un rol crucial în dezvoltarea acesteia. Un studiu recent, condus de Institutul de Tehnologie din Massachusetts și Universitatea Harvard tocmai a introdus un nou element în ecuație: genetica fiecărui individ.
Dintre diferitele studii de asociere efectuate până în prezent, regiunea genomică FTO este cea care prezintă o relație mai mare cu riscul de obezitate. Cu toate acestea, modul în care variația genetică din această regiune poate conferi vulnerabilitate la obezitate a fost încă o întrebare nerezolvată.
Prin analiza epigenomică a 127 de tipuri de celule umane, cercetătorii au găsit dovezi că tipul celular cel mai afectat de variația genetică la locusul FTO sunt progenitorii adipocitelor, celulele în care sunt depozitate grăsimile. Ei au identificat, de asemenea, un comutator genetic în regiune care reglementează genele IRX3 și IRX5. Prin compararea celulelor cu diferitele variante genetice, echipa a constatat că, în celulele progenitoare adipocitare, varianta de risc activează acest comutator - care este în mod normal oprit - și acest lucru la rândul său activează genele IRX3 și IRX5. Astfel, în timpul diferențierii adipocitelor, celulele care conțin varianta genetică de risc își repetă expresia genelor IRX3 și IRX5.
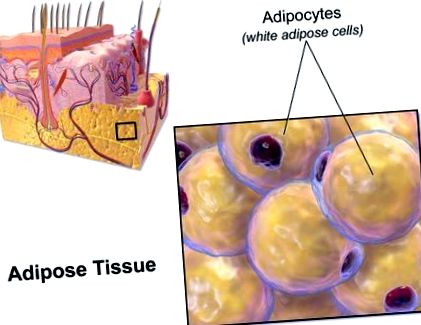
Țesut adipos. Personalul Blausen.com. «Galeria Blausen 2014». Wikiversity Journal of Medicine. DOI: 10.15347/wjm/2014.010. ISSN 20018762.
Echipa a stabilit că IRX3 și IRX5 sunt implicate în termogeneză, un proces prin care adipocitele disipă energia ca căldură, mai degrabă decât să o acumuleze ca grăsime. Astfel, în celulele cu varianta de risc, adipocitele suferă o tranziție de la celule capabile să disipeze energia la celule care acumulează energie, ducând la obezitate.
„Primele studii privind termogeneza s-au concentrat asupra țesutului de grăsime brună, care joacă un rol major la șoareci, dar este practic inexistent la oamenii adulți”, spune Melina Claussnitzer, primul autor al lucrării. Aceasta noua cale controleaza termogeneza in cele mai abundente rezerve de tesut adipos alb, iar asocierea sa genetica cu obezitatea indica faptul ca afecteaza echilibrul energetic global la om.
Cercetătorii au descoperit, în celulele unui pacient, că editarea genomului pentru a înlocui varianta de risc cu varianta non-risc a dezactivat din nou comutatorul genetic, restabilind reprimarea IRX3 și IRX5 astfel încât programul de exprimare a genelor legate de disiparea energiei iar termogeneza restaurată.
În plus, au observat că atât în celulele umane cât și în celulele de șoarece efectele variantei genetice ar putea fi inversate acționând asupra expresiei IRX3 sau IRX5. „Prin manipularea noii rute, am reușit să schimbăm programele de stocare și disipare a energiei la nivel celular și la nivelul întregului organism, oferind o nouă speranță pentru o vindecare împotriva obezității”, a declarat Manolis Kellis, directorul lucrării.
Rezultatele lucrării reprezintă, în primul rând, o schimbare importantă a modului de abordare a obezității, deoarece o mare parte din studiile anterioare au considerat că acțiunea variantei de risc în FTO ar avea loc asupra circuitelor nervoase care controlează apetitul. impactul său asupra progenitorilor adipocitelor indică existența unor căi independente de la creier. În plus, acestea oferă noi căi de acțiune terapeutică pentru tratamentul obezității. „Cunoașterea variantei cauzale implicate în asocierea obezității ar putea permite editarea genomului în celulele somatice ca o cale terapeutică pentru indivizii care prezintă alela de risc”, spune Kellis. Dar, mai important, circuitele celulare descoperite ne-ar putea permite să reglăm un comutator metabolic principal la persoanele cu risc și non-risc pentru a contracara contribuțiile de mediu, stilul de viață sau genetic la obezitate.
Referinţă: Claussnitzer M și colab. Circuitul variantei obezității FTO și rumenirea adipocitelor la oameni. N Engl J Med. 2015 3 septembrie; 373 (10): 895-907. doi: 10.1056/NEJMoa1502214.
- Genetica și mediul în obezitatea infantilă, conferință de Ángel Gil Hernández Agenda
- GĂSEȘTE MUTARE GENETICĂ ASOCIATĂ CU OBEZITATE; SOCHOB
- Obezitate: genetică sau obiceiuri slabe Prima-Derm
- Predispoziția genetică ar putea explica 60% din riscul obezității, potrivit experților
- Sensibilitatea genetică la hipertensiune arterială și obezitate scurtează durata de viață