1 Spitalul Institutului de Cercetări 12 de Octubre (i + 12) - Facultatea de Medicină - Universitatea Complutense din Madrid (Spania)
Pe de altă parte, incidența cancerului tiroidian diferențiat, un model experimental in vivo de supresie a hormonilor tiroidieni prin terapia preventivă a recidivelor, a crescut semnificativ. Există orientări clinice pentru gestionarea acestuia, dar este evident că posibilele efecte secundare derivate din aceasta necesită o indicație precisă ajustată la raportul risc-beneficiu al dozei de hormoni tiroidieni, prescris pe termen lung, în special în cazurile de tumori scăzute agresivitate, vârstă avansată și chiar la pacienții fragili. Pacienții cu risc crescut ar trebui să fie îndrumați pentru o densitometrie osoasă, pentru a lua în considerare tratamentul fracturilor viitoare. Prevenirea osteoporozei, în special la femeile aflate în postmenopauză, este extrem de dorită și ar trebui să includă o dietă adecvată în suplimentarea cu calciu și vitamina D, dacă este necesar. Nu există încă un consens cu privire la tratamentul osteoporozei la pacientul cu cancer tiroidian și tratament supresiv, dar criteriile indicate pentru osteoporoza postmenopauză în general par aplicabile.
Cuvinte cheieВ cancer tiroidian diferențiat; densitometrie fotonică duală; densitatea minerală osoasă; scor osos trabecular; hipertiroidism și hipotiroidism subclinic; hormonul tirotrop
În ultimii ani, s-au înregistrat progrese în reglarea dezvoltării scheletului și menținerea masei osoase a adultului de către axul hipotalamus-hipofiză-tiroidă. Au fost efectuate studii privind efectul hormonilor tiroidieni asupra osteoblastelor, osteoclastului și condrocitului. Această cercetare a condus la o mai bună cunoaștere genetică a fiziologiei acțiunii celulare a acestor hormoni. Recent, au fost propuse posibile intervenții de deodinază D2 în osteoporoză. Legătura dintre demnitatea minerală osoasă, calitatea osoasă și riscul de fracturi cu hormoni tiroidieni la femeile aflate în postmenopauză sugerează un rol pentru acești hormoni, chiar și în limitele tiroidei normale, în aceste boli.
Pe de altă parte, incidența cancerului tiroidian diferențiat, supresia experimentală in vivo a hormonilor tiroidieni prin terapie, boala recurentă, a crescut semnificativ. Există ghiduri de management, dar este clar că derivații secundari necesită o indicație precisă ajustată la echilibru, raportul risc-beneficiu al dozei de hormon tiroidian, prescris pe termen lung, mai ales în cazurile de agresivitate tumorală scăzută, vârstă avansată și chiar la pacienții fragili. Pacienții cu risc ridicat ar trebui să fie îndrumați pentru o densitometrie osoasă, pentru a lua în considerare tratarea fracturilor viitoare. Prevenirea osteoporozei, în special la femeile aflate în postmenopauză, este extrem de dorită și ar trebui să includă o dietă adecvată în suplimentarea cu calciu și vitamina D, dacă este necesar. Încă nu există un consens cu privire la tratamentul osteoporozei la pacientul cu cancer tiroidian și tratament supresiv, dar criteriile indicate pentru osteoporoza postmenopauză par a fi aplicabile în general.
Cuvinte cheieВ cancer tiroidian; densitometrie cu fotoni duali; densitatea minerală osoasă; scor osos trabecular; hipertiroidism și hipotiroidism subclinic; hormon tirotrofic
Hormonii tiroidieni (HT) intervin în dezvoltarea scheletului, în dobândirea vârfului masei osoase și în menținerea remodelării osoase. Studiile clinico-epidemiologice indică faptul că atât deficitul de HT cât și excesul sunt asociate cu riscul de fracturi, considerând că eutiroidismul este esențial pentru funcționarea normală a remodelării osoase [1].
În această lucrare vom analiza acțiunile celulare ale HT asupra osului și, în special, modelul experimental in vivo de exces și suprimare a hormonului stimulator tiroidian (TSH) la pacienții cu carcinom tiroidian diferențiat (DTC) la femei. Pre și postmenopauză. La bărbații cu CDT, nu există studii longitudinale de calitate pentru analiza lor.
Hormoni tiroidieni și os
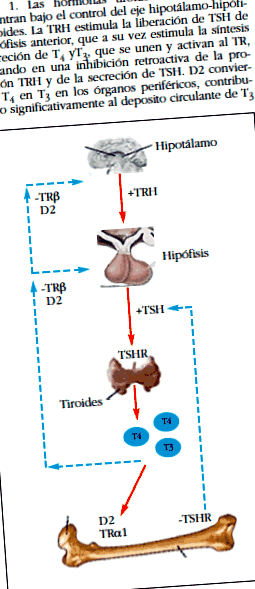
HT și osul sunt strâns legate, deoarece HT sunt regulatori cheie ai remodelării osoase. HT au un rol fundamental în creșterea și dezvoltarea vertebratelor. HT sunt iodotironine sintetizate în glanda tiroidă, a căror secreție constantă este asigurată de două mecanisme: 1) secreția de HT controlată printr-un mecanism retroactiv, de pe axa glandei hipotalamo-hipofizo-tiroidiene (Figura 1 și Figura 2) prin activare intracelulară reglementată de Deiodinaze iodotironine tisulare [2].
Fig2В T3 ar acționa indirect asupra osteoclastului printr-o acțiune mediată de osteoblast, inducând posibil eliberarea RANKL și interleukinele 6 și 8 și a PGE2, în stadii incipiente asupra precursorilor sau favorizând diferențierea preosteoclastului. T3 ar acționa favorizând diferențierea osteoblastului și fazele mineralizării matricei. Este posibil ca inducerea transcripției IGF-1 și a proteinelor sale transportoare și a altor factori să stimuleze proliferarea și diferențierea osteoblastului. Pe condrocit, disponibilitatea TRО ± 1 și TRОІ1 în această linie celulară, permite T3 să stimuleze maturarea acestuia și, prin urmare, procesul de osificare endocondrală. (Modificat din Wojcika și colab. 4) В
Receptoare pentru HT
Acești trei receptori funcționali pentru HTs (TRО ± 1, TRОІ1 și TRОІ2) sunt codificați de genele THRО ± și THRОІ, care reglează expresia și răspunsurile lor transcripționale la TR. În os, a fost descrisă expresia TRО ± 1 și TRОІ1, prima fiind în concentrații predominante de 10: 1. Prin urmare, TRО ± este considerat a fi mediatorul fundamental al acțiunii T3 asupra osului [6].
HT, TSH și dezvoltarea osoasă
Atât receptorii TRО ± 1, cât și receptorii TRОІ1 sunt exprimați pe condrocitele plăcii de creștere, sugerând că sunt ținte pentru acțiunea T3. Proliferarea și diferențierea condrocitelor este controlată de ariciul indian, PTHrp, BMP-R1A, IGF1, Wnt și FGF. Primele trei printr-un feedback negativ care induce creșterea plăcii și inhibă diferențierea acesteia prin controlul creșterii sale liniare. HT-urile intervin în această reglementare, sensibile la disponibilitatea T3, care stimulează exprimarea genelor pentru sinteza matricei cartilajului și a mineralizării sale ulterioare.
O mutație heterozigotă a genei THRО ± a fost descrisă recent la o fetiță de 6 ani, care, în ciuda faptului că prezintă HT în limita scăzută sau normală și TSH normală, a avut întârziere a creșterii și implicare osoasă histologică similară cu hipotiroidismul, ceea ce implică o rolul acestor receptori TRО ± în dezvoltarea osului uman [10].
HT și TSH în raport cu densitatea minerală osoasă și fracturile la populația normală
Un istoric de hipertiroidism pare a fi un factor de risc. În studiul SOF (Study of Osteoporotic Fractures) efectuat la 192 de femei în vârstă cu urmărire de 4,1 ani, cea mai mare incidență a fracturii osteoporotice a fost înregistrată la pacienții care au avut în antecedente fracturi și/sau hipertiroidie [cincisprezece]. În acest studiu, nu s-au găsit dovezi care să asocieze nivelurile scăzute de TSH cu DMO scăzută. Autorii au ajuns la concluzia că hipertiroidismul poate reduce sau nu masa osoasă, dar că în studiul lor scăderea DMO nu a fost responsabilă de asocierea puternică dintre hipertiroidismul anterior și riscul de fractură de șold.
HT și TSH: relație cu densitatea minerală osoasă și fracturi la femeile cu disfuncție tiroidiană
Pe scurt, datele publicate indică faptul că, pentru a demonstra o cauzalitate clară, sunt necesare studii randomizate și controlate cu un număr semnificativ de pacienți și pentru a evalua dacă normalizarea nivelurilor de TSH în hipertiroidismul subclinic este asociată cu riscul de fractură. Datele sugerează că hipertiroidismul subclinic este asociat cu un risc crescut de fracturi de șold și non-vertebrale, dar ar trebui analizați alți factori și efectuate studii de calitate superioară.
Microarhitectura trabeculară HT și osoasă
Criterii pentru suprimarea TSH în cancerul tiroidian diferențiat
Carcinomul tiroidian diferențiat (DTC) este cea mai frecventă neoplazie endocrină (reprezintă 1% din toate cazurile de cancer). 85-90% din cancerele tiroidiene sunt CDT, care include două variante, carcinom papilar (cel mai frecvent) și folicular. Incidența sa a crescut în ultimii 10 ani, dar mortalitatea sa a rămas aceeași [29]. Această creștere se datorează în mare parte creșterii și îmbunătățirii rezoluției testelor de diagnostic, cu o detecție mai mare a microcarcinomului incidental.
Tab1В TSH vizează terapia pe termen lung cu hormoni tiroidieni în carcinomul tiroidian diferențiat. Potrivit Haugen BR et al.32В
Note2tab1 ** Ținta TSH pentru pacienții cu răspuns biochimic incomplet poate varia în funcție de riscul inițial de ATA, nivelurile de Tg, tendința Tg în timp și riscul de suprimare.
Deși nu există un consens general cu privire la nivelurile optime de TSH pentru scăderea recidivelor și, în timp ce se minimizează efectele adverse ale hipertiroidismului subclinic, recent Asociația Americană a Tiroidei (ATA) a definit impactul suprimării TSH la pacienții cu CDT. Caracterizat prin scăzut, intermediar și ridicat riscul de recurență, luând în considerare diverși factori clinici [32].
Tab2В Lista studiilor longitudinale cu privire la efectul suprimării TSH cu levotiroxină asupra densității minerale osoase (BMD) la femeile pre și postmenopauză cu cancer tiroidian
Tratament supresiv cu HT în cancerul tiroidian și os diferențiat. Longitudinal vs. secțiuni transversale
Al doilea studiu longitudinal analizat este cel al lui Mulller și colab. [57] Au studiat 15 femei pre-menopauză și 10 femei post-menopauzale în tratament supresiv cu T4 pentru o perioadă variabilă de 1,5 ani. Din acest grup, au ajuns la 24 de pacienți cu DTC, reevaluați cu DXA cu un interval de urmărire de 1,5 ± 0,5 ani. Aceștia au selectat 15 subiecți martori identici cu sexul, starea menopauzei, vârsta și IMC. Ei au concluzionat că suprimarea TSH a fost însoțită de reduceri nesemnificative (2-5%) în BMD lombară și BMD gâtului femural, fără fracturi incidente. Scăderea BMD constatată este mai mică decât clasicul descris de Mazess, în care riscul crescut de fractură vertebrală crește de 1,5-2 ori pentru fiecare abatere standard (SD) pe care BMD o scade [58], ceea ce sugerează că nu există niciun efect la acest nivel.
Din experiența noastră [55], am studiat 14 femei pre-menopauzale și 13 post-menopauzale cu supresie CDT și TSH urmate în serviciul nostru de la tiroidectomia lor totală cu densitometrie repetată cu fotoni duali timp de doi ani. 50% dintre pacienții noștri au prezentat un TSH sub 0,1 mIU/L. Doza de LT4 a arătat o valoare predictivă pozitivă în fiecare situs osos studiat, care abia fusese descrisă. Niciunul dintre parametrii oaselor și mineralelor studiați nu a fost corelat cu masa osoasă, cu excepția fosfatazei alcaline la nivelul triunghiului lui Ward și a razei ultradistale. Acest lucru este în concordanță cu valorile normale ale DMO și remodelare osoasă găsite la acești pacienți cu tratamente supresive prelungite. Pacienții suprimați au prezentat o mică reducere a DMO în 1/3 distală a razei (scor Z = -0,77 ± 0,98; 95 CI: -1,11; -0,44), fără diferențe între pre și post menopauză.
Într-un grup selectiv și destul de mare de pacienți postmenopauzi cu CDT papilar, Sugitani și colab. [63] a analizat efectul pe care terapia supresivă TSH postoperatorie îl induce asupra supraviețuirii fără boală și efectele sale asupra DMO. Au analizat două grupuri: 140 de pacienți cu supresie (TSH medie: 0,07 ± 0,10 mIU/L și 127 fără supresie (TSH medie: 3,14 ± 1,60 mIU/L). urmat timp de 5 ani, arătând o scădere a DMO lombare la subgrupul de femei în postmenopauză cu vârsta peste 50 de ani. Majoritatea pacienților lor prezintă un risc scăzut. La final recomandă suprimarea TSH, în special la pacienții cu risc scăzut și pacienții vârstnici, nu ar trebui indicat, ținând cont de faptul că nu s-a demonstrat că scade recurențele chiar și la pacienții cu risc.
Studiul longitudinal realizat de Karner și colab. [64] a fost efectuată la femeile în premenopauză cu CDT timp de un an. Durata suprimării TSH la începutul studiului a fost de 9,4 ± 6,4 ani și, prin urmare, lungă. Măsurătorile DMO au fost efectuate de două ori pe o perioadă de un an. Folosind SPA (absorptiometria cu foton unic) pentru extremități și DXA, aceștia nu au constatat o scădere a DMO la nivelul razei distale și nici a DMO lombare și/sau de șold. Este un studiu longitudinal de scurtă durată, cu un număr mic de subiecți (19 premenopauză). Principala sa recomandare este de a efectua un studiu de densitometrie osoasă înainte de a începe tratamentul supresiv TSH pentru a identifica pacienții cu risc crescut de osteoporoză.
Factori de risc la pacienții cu tratament supresiv CDT și TSH
- Peste 25 de ani, obezitatea va provoca mai mult cancer decât fumatul la femei
- Experții subliniază că obezitatea este legată de cancerul tiroidian diferențiat de acest tip
- Histerectomia este o opțiune pentru femeile obeze cu cancer uterin Diario Público
- Eficacitatea tratamentului hormonal la femeile la menopauză cu cancer de sân depinde de greutate
- Obezitatea dublează riscul de cancer de colon la femeile CuidatePlus