Asociația spaniolă de pediatrie are ca unul dintre obiectivele sale principale diseminarea informațiilor științifice riguroase și actualizate despre diferitele domenii ale pediatriei. Anales de Pediatría este Corpul de Expresie Științifică al Asociației și constituie vehiculul prin care comunică asociații. Publică lucrări originale despre cercetarea clinică în pediatrie din Spania și țările din America Latină, precum și articole de revizuire pregătite de cei mai buni profesioniști din fiecare specialitate, comunicările anuale ale congresului și cărțile de minute ale Asociației și ghidurile de acțiune pregătite de diferitele societăți/specializate Secțiuni integrate în Asociația Spaniolă de Pediatrie. Revista, un punct de referință pentru pediatria vorbitoare de limbă spaniolă, este indexată în cele mai importante baze de date internaționale: Index Medicus/Medline, EMBASE/Excerpta Medica și Index Médico Español.
Indexat în:
Index Medicus/Medline IBECS, IME, SCOPUS, Science Citation Index Expanded, Journal Citations Report, Embase/Excerpta, Medica
Urmareste-ne pe:
Factorul de impact măsoară numărul mediu de citații primite într-un an pentru lucrările publicate în publicație în ultimii doi ani.
CiteScore măsoară numărul mediu de citări primite pentru fiecare articol publicat. Citeste mai mult
SJR este o valoare prestigioasă, bazată pe ideea că toate citatele nu sunt egale. SJR folosește un algoritm similar cu rangul de pagină Google; este o măsură cantitativă și calitativă a impactului unei publicații.
SNIP face posibilă compararea impactului revistelor din diferite domenii de subiecte, corectând diferențele de probabilitate de a fi citate care există între revistele de subiecte diferite.
Descris pentru prima dată în 1964 1, sindromul Shwachman-Diamond (SSD) este o boală autozomală recesivă rară, cu o incidență aproximativă de 1 din 100.000 de nașteri 2,3 și un raport bărbat-femeie de 1,7: 1 3, 4. Este a doua cauză a insuficienței pancreatice exocrine congenitale în copilărie după fibroza chistică.
SSD este o boală multisistemică caracterizată prin insuficiență pancreatică exocrină, disfuncție a măduvei osoase, alterări ale scheletului și statură scurtă 2,5-8. Prognosticul pacienților este determinat de infecțiile bacteriene recurente, secundare în principal alterării neutrofilelor, precum și de disfuncția coloanei vertebrale și leucemie.
Gena SBDS a fost identificată recent ca gena responsabilă pentru SSD. Această genă a fost localizată la nivelul cromozomului 7, la locul 7q11 5,9,10 .
În acest articol vom descrie cazul clinic al unui sugar care a fost diagnosticat cu acest sindrom în serviciul nostru.
Un sugar de 14 luni este trimis la serviciul nostru pentru un studiu al hipertransaminazemiei și stagnării în greutate de la vârsta de 9 luni.
Copilul nu a prezentat nicio istorie familială sau personală relevantă. Greutatea la naștere a fost de 3.390 g și înălțimea de 51 cm. El a prezentat o dezvoltare adecvată a greutății statutare până la vârsta de 9 luni, moment în care a început să aibă 4-5 scaune lipicioase, cu miros rânced pe zi, împreună cu stagnarea greutății legale.
Ca urmare a afecțiunii, medicul pediatru a efectuat o analiză în care s-au remarcat doar un GOT de 464 U/l și un GPT de 514 U/l. De asemenea, a avut niște markeri de boală celiacă care erau normali.
Trei luni mai târziu, din cauza persistenței hipertransaminazemiei, a fost trimis la serviciul nostru pentru studiu.
Examenul fizic a relevat un aspect microsomal armonic, cu o greutate și înălțime sub percentila 3. Restul examinării a fost normal.
Testele complementare efectuate au fost următoarele:
Hemogramă: 8.400 leucocite (N, 16%; L, 77%; M, 5,8%), hematocrit 34,6%, hemoglobină 11,6 g/dl și 313.000 trombocite.
Biochimie generală: GOT, 417 U/l; GPT, 440 U/L; bilirubină normală, GGT și fosfatază alcalină.
Test de transpirație normală.
Van de Kamer: fără steatoree. Scaun elastaz 11,5 μg/g.
Serologii de hepatită virală, 1-antitripsină, metabolism normal al cuprului și zincului.
Ecografie abdominală: hiperdensitate pancreatică foarte marcată care sugerează insuficiența pancreatică exocrină.
În rezumat, am găsit o imagine a insuficienței pancreatice exocrine diagnosticată de o elastază practic nedetectabilă în scaun și un studiu cu ultrasunete compatibil, cu un test de transpirație normal repetat de două ori. În plus, copilul a avut întârzierea creșterii și neutropenie ușoară. Cu suspiciunea unui SSD, am procedat la efectuarea unui studiu osos radiologic normal și a unui studiu genetic care a determinat că copilul era un heterozigot compus din două mutații ale genei SBDS (258 + 2T> C/183-184TA> CT) cu care punem diagnosticul SSD la copil.
Un studiu genetic a fost, de asemenea, efectuat la părinți, având ca rezultat tatăl purtând mutația TA> CT 183-184 și mama purtând mutația 258 + 2T> C.
Având în vedere diagnosticul, a fost început tratamentul cu enzime pancreatice și vitamine liposolubile, îmbunătățind aspectul scaunului, dar nu și dezvoltarea greutății, menținând greutatea și înălțimea sub percentila 3.
Numărul de neutrofile a variat, ajungând la cifre de 540 de neutrofile.
Fenotipul clinic al SSD este foarte eterogen, prezentând o mare varietate de manifestări clinice. Trăsăturile centrale ale sindromului sunt insuficiența pancreatică exocrină și disfuncția măduvei spinării, ambele esențiale pentru stabilirea diagnosticului 2,11. În mod similar, întârzierea creșterii și modificările scheletice sunt caracteristice 2,11,12 .
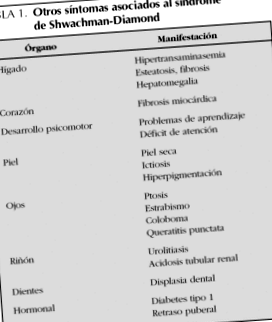
Alte posibile descoperiri în SSD sunt enumerate în Tabelul 1. Modificările pielii, ochiului și rinichilor sunt foarte rare.
Primele simptome și semne ale SSD apar de obicei în primul an de viață, așa cum este cazul pacientului nostru 3 .
Când diagnosticul este pus în copilărie, disfuncția pancreatică este prezentă în practic toate cazurile. Concentrațiile scăzute de amilază (50-75% dintre pacienți), tripsinogenul seric scăzut (70-98%) și testul de stimulare pancreatică modificată (100%) sunt tipice 2,4. În prezent, determinarea elastazei fecale este cel mai eficient test pentru evaluarea insuficienței pancreatice, datorită specificității și sensibilității sale ridicate și deoarece valorile sale nu sunt modificate prin luarea enzimelor pancreatice. Insuficiența pancreatică severă este considerată a fi un nivel de elastază scaun mai mic de 100 μg/g de scaun 3. În ceea ce privește studiile imagistice, ecografia abdominală prezintă un pancreas de dimensiuni normale sau scăzute, cu ecogenitate crescută. CT relevă lipomatoza pancreatică 14. În cazul nostru, diagnosticul a fost pus cu o elastază de scaun de 11,5 μg/g, împreună cu ultrasunete sugestive.
Implicarea pancreatică se îmbunătățește de obicei odată cu vârsta în 40-60% din cazuri, aparent datorită creșterii secreției de lipază cu vârsta de 2,8 .
Cea mai frecventă constatare hematologică este neutropenia intermitentă care apare în 85-100% din cazuri 2,15,16. Indiferent de numărul total de neutrofile, există și o modificare a migrației acestora, motiv pentru care există un risc crescut de infecții bacteriene grave chiar și cu un număr normal de neutrofile 11,17. Apariția infecțiilor determină prognosticul în copilărie 18. Copilul nostru a prezentat cifre de până la 500 de neutrofile în evoluția sa, care s-au recuperat spontan.
Alte modificări hematologice care pot fi găsite sunt anemia (50-80%), concentrațiile crescute de hemoglobină fetală (80%) și trombocitopenia (25-85%) 15,19 .
Întârzierea creșterii apare la 60% dintre copii și este independentă de malabsorbția digestivă, deoarece nu se îmbunătățește cu suplimentarea enzimei pancreatice și nici cu normalizarea funcției pancreatice care poate apărea odată cu vârsta. Înălțimea și greutatea sub 3 8,15 percentile sunt tipice. Întârzierea pare a se datora unei probleme inerente de creștere 2. Cazul nostru nu a prezentat o îmbunătățire a înălțimii în acest moment, în ciuda suplimentării enzimelor pancreatice și este monitorizat în cadrul consultației endocrinologice pentru a monitoriza evoluția înălțimii.
Modificările osoase pot apărea la 50-75% dintre pacienți, deși un articol recent care analizează modificările radiologice la 15 pacienți constată modificări la practic toți pacienții 12. Cele mai frecvente constatări sunt coastele scurte cu îngroșare costocondrală, o îngustare a cuștii toracice, mai evidentă la copiii cu vârsta sub 2 ani și condrodisplazia metafizară a oaselor lungi (în special la șolduri și genunchi) 11, mai evidentă la copiii cu vârsta peste 2 ani. ani de vârstă.6 ani. Alte constatări sunt: apariția întârziată a centrelor secundare de osificare, osteopenia generalizată, tubulația anormală a oaselor lungi, în special tibia și prima metacarpiană, clinodactilia, sindactilia și deformările valgului genunchilor și șoldurilor. La copilul nostru, nu au apărut modificări în seria osoasă care a fost efectuată, ceea ce se poate datora faptului că copilul era foarte mic în momentul în care a fost efectuat.
Alte descoperiri posibile sunt transaminazele crescute și hepatomegalia, care sunt de obicei prezente în primii ani de viață și, de obicei, se îmbunătățesc fără complicații odată cu vârsta. În cazul nostru, hipertransaminazemia a fost motivul trimiterii la consultația noastră.
Studii recente arată că mutațiile genei SDBS sunt prezente la majoritatea pacienților cu SSD 9,20. Această genă a fost localizată pe cromozomul 7, la locusul 7q11. Cele două mutații identificate cel mai frecvent în literatura medicală în gena SBDS (183-184 TA x CT [K62X] și IVS2 (258) + 2T x C [C84fs], coincid cu cele prezentate de copilul nostru 5,21,22. Fiecare dintre părinți au fost purtători ai uneia dintre cele două mutații descrise.
În ceea ce privește tratamentul, intervențiile se vor desfășura pe următoarele linii:
1. Suplimentarea enzimelor pancreatice și a vitaminelor liposolubile.
2. Prevenirea și tratamentul bolilor infecțioase invazive cu tratamentul precoce al bolilor febrile.
3. Corectarea anomaliilor hematologice atunci când este posibil.
4. Urmărirea și tratamentul deformărilor ortopedice.
Neutropenia severă sau infecțiile recurente pot fi tratate cu factor de stimulare a coloniei de granulocite (G-CSF) 16. Cu toate acestea, există controverse cu privire la posibilitatea accelerării dezvoltării sindroamelor mieloproliferative 2,11 .
Transfuziile pot fi necesare la pacienții cu anemie sau trombocitopenie simptomatică. Eritropoietina poate fi, de asemenea, utilă în tratarea anemiei.
Hormonul de creștere a fost încercat fără rezultate bune pe termen lung 23 .
Transplantul de măduvă osoasă este singura opțiune curativă pentru disfuncția severă a măduvei spinării și este recomandat la pacienții cu pancitopenie severă și sindroame limfoproliferative și mieloproliferative 11,24-26 .
Prognosticul acestei boli este determinat de infecțiile 27 și de apariția proceselor neoplazice hematologice. Cele mai frecvente transformări sunt mieloide acute, limfoide acute și leucemie mieloidă cronică juvenilă 2,3,7. Acest risc de malignitate este estimat la aproximativ 25% 3,4. Riscul este mai mare la copiii cu pancitopenie progresivă. Supraviețuirea mediană a acestor pacienți este estimată la aproximativ 35 de ani 28 .
- Urticaria de fr; sau și boala celiacă la pacientul pediatric; trico Annals of Pediatrics
- S; sindromul de microduplicare; n 3q29 Analele pediatriei
- Recomandări nutriționale pentru copil; sau sportivul Annals of Pediatrics
- Tumori renale la ni; mai puțin de un an; o Analele pediatriei
- Tratamentul meningitei bacteriene Analele pediatriei