INTRODUCERE
Un adenom hipofizar care produce și secretă excesiv hormonul corticotropină (ACTH) produce un tablou clinic numit boala Cushing.
Persoanele cu boala Cushing au prea multă corticotropină, care la rândul său stimulează producția și secreția de cortizol de către glandele suprarenale (situate deasupra rinichilor). Acest exces de cortizol este cel care produce tabloul clinic.
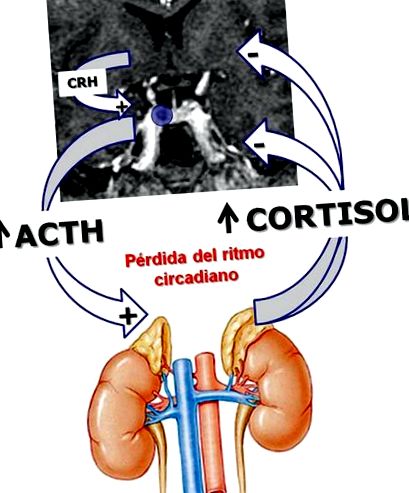
Trebuie remarcat faptul că în condiții normale atât ACTH cât și ulterior cortizolul sunt secretate în impulsuri pe tot parcursul zilei (vârful maxim de secreție fiind în jurul orei 8 a.m.). Ce se întâmplă în boala Cushing este că ritmul de secreție se pierde în impulsuri (ritm circadian), rezultând o producție endogenă mai mare de cortizol pe tot parcursul zilei.
Cortizolul, cunoscut și sub numele de hormonul stresului, are printre principalele sale funcții normale: reglarea nivelului de glucoză din sânge (gluconeogeneză); participă la metabolismul lipidelor, glucidelor și proteinelor; reglează homeostazia apei și a ionilor (acțiune mineralocorticoidă); modulează sistemul imunitar; controlează tensiunea arterială și formarea oaselor.
Excesul de corticosteroizi din sânge produce un tablou clinic numit sindrom Cushing, care poate avea cauze multiple. Când sindromul Cushing este cauzat de un adenom hipofizar care secretă ACTH, acesta se numește boala Cushing. Harvey Cushing a fost un neurochirurg distins al secolului trecut care a descris sindromul și boala care îi poartă numele.
Tipul de adenom hipofizar care secretă ACTH este cunoscut sub numele de corticotropinom și reprezintă aproximativ 10% din totalul adenoamelor hipofizare din practica medicală.
Boala Cushing este foarte rară, cu o incidență de 0,7 până la 2,4 cazuri noi pe milion de locuitori pe an.
Există o tendință mai mare să apară la femei într-o proporție între 5 și 15 ori mai mare decât la bărbați. Vârsta de debut este cuprinsă între 20 și 50 de ani, fiind foarte rară la copii și adolescenți.
Este important de știut că în momentul diagnosticului, aproximativ 85% din adenoamele care cauzează boala Cushing sunt microadenoame (mai mici de 10 mm), astfel încât rezultatele unei intervenții chirurgicale transfenoidale transnazale sunt favorizate, aceasta fiind prima opțiune terapeutică.
Harvey Cushing (1869-1939)
PREZENTARE CLINICĂ
Tabloul clinic este cel al sindromului Cushing și este compus din:
Modificări și simptome fiziognomice
- Obezitate abdominală cu brațe și picioare subțiri (obezitate centripetă).
- Față rotundă (față de lună plină).
- Pletora facială, acnee și hirsutism.
- Acumularea de grăsime între umeri (cocoașă dorsală) și la nivelul golului supraclavicular.
- Vergeturi roșii-venoase pe pielea abdomenului, coapselor și sânilor.
- Pielea subțire predispusă la vânătăi spontane fără legătură cu traume.
- Telangiectazii.
- Creșterea excesivă a părului pe față, gât, piept, abdomen și coapse.
- Alopecia la femei.
- Dificultăți de vindecare a rănilor cutanate.
- Infecții fungice oportuniste ale pielii și unghiilor.
- Acanthosis nigricans.
- La nivelul sistemului nervos: anxietate și insomnie, depresie, deficit de memorie și atenție, imagini de euforie sau psihoză.
- La nivel ocular: glaucom și/sau cataractă.
- La nivel gastro-intestinal: ulcer peptic.
- La nivel sanguin: anemie, boală tromboembolică, imunosupresie, hipocalcemie, hipokaliemie.
- La nivel urinar: sete și urinare crescute (polidipsie și poliurie); pietre la rinichi.
- La nivel reproductiv: oligo-amenoree și infertilitate (femei); libidoul redus, impotența și infertilitatea (bărbați).
- La nivel locomotor: slăbiciune musculară marcată și oboseală în special la nivelul mușchilor proximali, dureri articulare și osteoporoză (fracturi spontane de coastă și coloană vertebrală).
Modificări metabolice și/sau funcționale
- Hipertensiune arteriala.
- Obezitatea.
- Rezistența la insulină sau Diabetul zaharat.
- Dislipidemie.
- Hipokaliemie și hipocalcemie.
- Imunosupresia.
Clinică legată de efectul compresiv al adenomului
- Cefalee (cefalee).
- În cazul macroadenoamelor (foarte rare în boala Cushing) pot exista: tulburări de vedere, hiperprolactinemie datorată „efectului stem” și/sau hipopituitarismului.
Unele dintre semnele și simptomele clinice sunt tipice sindromului Cushing și pot duce la suspiciuni diagnostice, acestea fiind: vergeturi roșii-venoase, pletora feței, slăbiciune musculară proximală, piele subțiată, vânătăi spontane și osteoporoză de cauză incertă.
DIAGNOSTIC
Diagnosticul final al bolii Cushing nu este simplu și necesită studii multiple care sunt efectuate într-o manieră eșalonată și, frecvent, este necesar să le repetați de mai multe ori pentru a ajunge la diagnosticul corect. Interpretarea rezultatelor ar trebui lăsată la o neuroendocrinolog cu experiență, pentru a evita erorile de interpretare și erorile în tratament.
Laboratorul hormonal
Primul lucru care trebuie făcut atunci când există suspiciunea clinică a sindromului Cushing este confirmarea acestuia printr-o serie de studii de laborator. Aceste studii determină dacă există o producție mare de cortizol de către organism. Două sau mai multe dintre următoarele teste pozitive sunt necesare pentru a determina sindromul Cushing:
Odată ce diagnosticul sindromului Cushing a fost făcut cu testele de laborator descrise, este necesar să se determine dacă cauza este boala Cushing, adică un adenom în glanda pituitară; sau dacă cauza este alta și se găsește într-o altă parte a corpului în afara hipofizei. Pentru aceasta este necesar să continuați cu următoarele analize hormonale:
Rezonanța magnetică a hipofizei cu gadoliniu
Când se confirmă de către laboratoarele hormonale că cauza sindromului Cushing este un adenom hipofizar; Cu alte cuvinte, ceea ce se numește boala Cushing, pasul următor este efectuarea unui RMN cu gadoliniu concentrându-se pe glanda pituitară. Astfel, va fi posibil să se evalueze dacă unul este în prezența unui microadenom (cel mai frecvent, 85%) sau a unui macroadenom (15%).
În prezent există echipamente de imagistică prin rezonanță magnetică cu o putere de 3 Teslas care permit detectarea microadenoamelor foarte mici de doar câțiva milimetri, care pot trece neobservate în secvențele de rezonanță dinamică realizate cu echipamente cu putere redusă.
Cu toate acestea, dacă microadenomul nu poate fi detectat cu precizie la RMN sau există îndoieli cu privire la interpretarea acestuia, este necesar să se confirme diagnosticul bolii Cushing printr-o cateterizare a sinusurilor petrosale inferioare.
Cateterizarea sinusului petrosal inferior
Se efectuează la unii pacienți la care este necesar să se confirme diagnosticul bolii Cushing din cauza faptului că RMN nu este concludent.
Obiectivul este de a putea confirma secreția de ACTH în sângele venos (în special către sinusurile petrosale inferioare) printr-un adenom corticotrop care nu poate fi identificat corect în imagistica prin rezonanță magnetică.
Este un studiu invaziv care se realizează prin cateterizarea ambelor vene femurale la nivel inghinal și apoi urcă cu cateterul până ajunge la baza craniului, plasând capătul cateterului la nivelul ambelor sinusuri petrosale inferioare pe fiecare lateral într-un simultan.
Două probe de sânge bazale sunt luate înainte de stimulare. Secreția de ACTH este apoi stimulată cu un medicament specific (cu CRH sau desmopresină) și se prelevează mai multe probe de sânge, amânate cu câteva minute. În toate aceste probe de sânge, reprezentând fiecare dintre sinusurile petrosale inferioare, ACTH se măsoară și se compară cu ACTH obținut în sângele periferic (dintr-o venă din braț)
Gradul ACTH (diferența) dintre fiecare sinus petrosal inferior și sângele periferic este comparat. Testul este considerat pozitiv pentru un adenom hipofizar în oricare dintre următoarele două situații:
- Gradientul este mai mare sau egal cu 2 în eșantioanele de bază.
- Gradientul este mai mare de 3 după stimularea farmacologică.
Cateterizarea ar putea ajuta, de asemenea, la identificarea lateralizării unui adenom dacă gradientul dintre ambele sinusuri petrosale este mai mare de 1: 4.
Câmp vizual computerizat
În cazul în care un macroadenom este cauza bolii Cushing, care este foarte rară, este necesar să se determine dacă există vreun compromis în calea optică (chiasmă optică, nervi optici, tract optic). Imaginea tipică a pierderii câmpului vizual este cunoscută sub numele de hemianopie bitemporală și este cauzată de compresia chiasmei optice de către macroadenom.
TRATAMENT
Boala Cushing lăsată la libera evoluție produce o deteriorare rapidă a pacientului, care poate fi potențial fatală dacă nu este controlată cu o strategie terapeutică.
Studiile inițiale la pacienții cu boala Cushing au arătat că, fără un anumit tip de tratament, jumătate dintre pacienți ar putea muri din cauze cardiovasculare (infarct miocardic sau accidente vasculare cerebrale) sau din cauze infecțioase în primii cinci ani de boală. Din fericire, odată cu medicina actuală axată pe chirurgie și avansarea farmacologiei, aceste cifre au scăzut drastic.
Un tratament eficient îmbunătățește simptomele pacientului, calitatea vieții și speranța de viață.
Există mai mulți piloni în tratament: chirurgie, tratament medicamentos și radioterapie. Unii pacienți necesită o combinație a acestor modalități pentru un control adecvat al bolii.
Obiectivele tratamentului
- Stare de hipocortizolism (valori ale cortizolului sub normal):
Este starea ideală după operație. Este definit ca o reducere a cortizolului seric (dozat la 8 a.m.) și/sau C.L.U. 24 de ore sub limita inferioară a laboratorului de testare. - Starea eucortizolismului (valorile cortizolului în intervalul normal):
De asemenea, este considerată o realizare terapeutică. Este definit ca valorile serice ale cortizolului măsurate la 8 a.m. sau C.L.U. în limitele lor de normalitate. - Menținerea sau recuperarea funcției hipofizare.
- Reducerea morbidității și mortalității.
Chirurgie transnasală transfenoidală
Acesta continuă să fie prima opțiune terapeutică, deoarece poate obține remisiunea bolii Cushing în aproximativ 80% din cazuri.
Se subliniază faptul că această rată de succes chirurgical și riscul de complicații sunt direct legate de experiența neurochirurgului.
Tehnica obișnuită se realizează prin nas în ceea ce se numește chirurgie transnasală transfenoidală. Poate fi efectuat cu tehnici microchirurgicale sau prin endoscopie, în funcție de fiecare caz. Tehnica endoscopică este cea mai utilizată astăzi.
Chirurgia singură poate fi singurul tratament și control al bolii necesare, în special în acele microadenoame care nu invadează sinusul cavernos.
Majoritatea pacienților necesită tratament farmacologic înainte de operație (vezi mai jos) pentru a îmbunătăți simptomele înainte de operație și pentru a putea ajunge la o stare mai bună. Această decizie trebuie luată în comun între neurochirurg și endocrinolog în fiecare caz particular.
După operație, este de așteptat o stare de hipocartizolism, care se traduce printr-o oboseală marcată și decăderea pacientului. Acest scenariu este un bun parametru clinic pentru o intervenție chirurgicală reușită, dar trebuie gestionat prin înlocuirea cu glucocorticoizi orali (de obicei hidrocortizon) până când endocrinologul decide când trebuie întrerupt.
Pacient în vârstă de 20 de ani cu boală Cushing avansată din cauza unui microadenom hipofizar (săgeți albastre).
Același pacient ca și figura precedentă după o intervenție chirurgicală transnasală endoscopică. Rețineți îmbunătățirea clinică cu trecerea timpului și RMN, unde microadenomul nu mai este evident, doar glanda pituitară normală.
Farmacoterapie
În general, tratamentul farmacologic nu este prima opțiune a unui tratament definitiv. Este frecvent utilizat cu scopul de a îmbunătăți starea clinică a pacientului înainte de operație.
Pe de altă parte, dacă pacientul a suferit o intervenție chirurgicală și boala este încă activă din cauza unei rămășițe de adenom, poate fi necesar să reveniți la tratamentul farmacologic.
Există patru grupuri de medicamente disponibile, următoarele fiind cele mai utilizate astăzi:
- Medicamente cu acțiune inhibitoare a enzimelor glandei suprarenale: sunt cele care scad sinteza cortizolului de către glandele suprarenale. Nu au niciun efect asupra adenomului hipofizar.
- Ketoconazol
- Mitotan
- Etomidat
- LCI699 (în studiu)
- Medicamente cu acțiune adrenolitică: produce atrofie și necroză a celulelor cortexului suprarenal, locul unde se produc glucocorticoizi endogeni.
- Mitotan
- Medicamentele cu acțiune centrală: sunt cele care scad sinteza ACTH de către adenomul hipofizar și ar putea scădea dimensiunea adenomului. Cele care s-au dovedit a fi eficiente și sunt disponibile comercial sunt:
- Agoniștii dopaminei: cabergolina
- Analogi de somatostatină: pasireotidă
- Medicamente cu acțiune antagonistă a receptorilor glucocorticoizi: sunt cele care blochează acțiunea glucocorticoizilor la nivel celular în tot corpul
- Mifepristonă
Radioterapie
În cazul adenoamelor corticotrope care produc boala Cushing, utilizarea radioterapiei este rezervată exclusiv acelor cazuri în care boala este încă activă datorită unor resturi de adenom, care nu au putut fi controlate prin intervenții chirurgicale sau printr-un tratament farmacologic adecvat. Radioterapia hipofizară nu este niciodată prima linie de tratament în boala Cushing și ar trebui indicată cu atenție printr-un consens între endocrinolog și neurochirurg. În plus, trebuie avut în vedere faptul că rezultatul radioterapiei poate fi observat după câțiva ani după ce a fost efectuată, astfel încât pacientul trebuie să continue tratamentul medicamentos în acea perioadă. Modalitățile de radioterapie în prezent sunt: radioterapia stereotactică sau radioterapia stereotactică fracționată.
Suprarenalectomie bilaterală
Unii pacienți foarte atent selectați în care intervenția chirurgicală, tratamentul medical și radioterapia au eșuat, iar tabloul clinic este foarte sever, pot necesita o suprarenalectomie laparoscopică bilaterală (rezecția ambelor glande suprarenale). Pacienții încetează să producă hormoni suprarenali, de aceea este necesară terapia pe tot parcursul vieții cu glucocorticoizi și mineralocorticoizi.
O posibilitate nedorită la un pacient cu suprarenalectomie este dezvoltarea sindromului Nelson: creșterea necontrolată a adenomului hipofizar rezidual într-un macroadenom, care poate apărea la 30% dintre pacienți (deși cu mai puține posibilități la cei iradiați anterior).
- Sudoarea engleză, boala misterioasă care i-a afectat pe bogați și tocmai a dispărut
- Tratamentul bolii celiace poate inversa insuficiența hepatică - Știri medicale
- Arterita lui Takayasu, o boală care dăunează vaselor de sânge
- FDA din Statele Unite investighează relația dintre alimentele pentru animale de companie și bolile de inimă
- Grâul poate fi făcut sigur pentru persoanele cu boală celiacă prin editarea genelor