Rev Chil Pediatr 2007; 78 (2): 169-175
CAZ CLINIC
RAPORT DE CAZ
Pancreatită acută recurentă, caz clinic
Pancreatită acută recurentă
PAMELA ARGOLLO M. 1 , CRISTIAN GARCÍA B. Două , PAUL R. HARRIS D. 3
1. Rezident în pediatrie, Pontificia Universidad Católica de Chile. Departamentul de Pediatrie. Facultatea de Medicină, Pontificia
Universitatea Catolică din Chile.
Două . Departamentul de Pediatrie și Radiologie. Facultatea de Medicină, Pontificia Universidad Católica de Chile.
3. Departamentele de pediatrie. Facultatea de Medicină, Pontificia Universidad Católica de Chile.
fundal: Pancreatita acută recurentă (RAP) este definită ca episoade de pancreatită acută cu rezoluție clinică și anatomică completă între fiecare episod. Etiologia este diversă la copii (20-35% necunoscută). Obiectiv: Analizați etiologia, diagnosticul și cel mai adecvat screening al RAP la copii. Raport de caz: Un băiat de 9 ani cu 6 episoade de pancreatită acută (AP); 4 dintre ei au necesitat internarea în spital. Studiul a inclus o colangiopancreatografie normală, examene imunologice și metabolice de bază normale și evaluarea genetică negativă a celei mai frecvente mutații a fibrozei chistice. În timpul episoadelor de AP, s-au obținut 3 imagini de tomografie computerizată și au prezentat AP în diferite grade (Baltasar C și E). Testarea genetică a pancreatitei ereditare a fost negativă. S-a efectuat colecistectomie laparoscopică. Concluzie: RAP trebuie suspectat la copiii cu dureri abdominale recurente și concentrație crescută de amilază-lipază serică, pentru a iniția o evaluare adecvată.
(Cuvinte cheie: pancreatită recurentă, litiază biliară, pancreatită ereditară).
(Cuvinte cheie: pancreatită recurentă, calculi biliari, pancreatită ereditară).
Introducere
Pancreatita acută recurentă (RAP) este definită ca episoade recurente de AP cu rezoluție clinică completă între imagini și cu recuperare completă a parenchimului pancreatic. Episoadele recurente de AP pot duce la pancreatită cronică, cu afectarea structurală a sechelelor și la un factor de risc asociat pentru adenocarcinomul pancreatic 4, 6 .
Obiectivul acestei lucrări a fost de a discuta diagnosticul etiologic al PAR în pediatrie și cel mai adecvat studiu, pentru care prezentăm cazul unui copil cu PAR.
Caz clinic
Un băiat de 9 ani, în vârstă de 8 luni, cu antecedente de obezitate (IPT: 139%, IMC: 23,5) și 6 episoade de AP, dintre care 2 au fost gestionate în ambulatoriu. Primul episod la vârsta de 6 ani. În raport cu primele 3 episoade de PAR, a fost inițiat un studiu etiologic în care s-au evidențiat următoarele: ultrasonografie abdominală (SUA) cu vezică biliară fără litiază, duct biliar intra- și extrahepatic nedilatat, colangiopancreatografie cu rezonanță magnetică (MRCP) fără patologie constatări, bila prin duodenal sunând negativ pentru cristalele de colesterol sau microlitiaza colesterolului, dar prezentând granule de bilirubinat de calciu care ar putea fi asociate cu pietre pigmentare în conducta biliară.
Cu pacientul în condiții clinice stabile, studiul etiologic a fost completat cu o evaluare imunologică normală (anti-ADN, ANCA, factor reumatoid, anticorpi antinucleari și imunoglobuline serice). În plus, a fost solicitat un test de transpirație, care a fost normal (32 mEq NaCl) și un studiu de mutație pentru fibroza chistică care nu a arătat nicio mutație în cadrul celor 29 de mutații studiate. El este externat în stare generală bună, asimptomatic și cu ultimul control al lipazei la 104 U/l.
Din cauza istoricului de PAR, a absenței etiologiei identificabile și a luării în considerare a riscurilor, sa decis efectuarea unei colecistectomii elective care se efectuează laparoscopic la 45 de zile după episodul 4 al AP, găsind o vezică biliară distendată, fără litiază, al cărei studiu histologic posterior a fost normal.
La două luni după colecistectomia profilactică, ea a prezentat un nou episod de durere abdominală nespecifică, localizată în epigastru, fără radiații și mai târziu vărsături biliare și diaree apoasă fără elemente patologice. Enzimele sale pancreatice s-au găsit crescute (amilază: 230 U/I și lipază: 496 U/I), motiv pentru care s-a decis spitalizarea sa, evoluând satisfăcător, cu scăderea durerii, fără noi episoade de vărsături. Odată stabil și cu lipază serică de 145 U/I, a fost externat cu un tratament pe bază de enzime pancreatice (Creon®) în încercarea de a reduce secrețiile pancreatice prin feedback negativ prin scăderea secreției de secretină/CCK la nivel duodenal.
După cel de-al cincilea episod și fiind asimptomatic, s-a efectuat MRCP, care nu a prezentat modificări anatomice ale canalului biliar sau ale canalelor pancreatice, în special fără dovezi ale pancreasului divizat (Figura 2).
În același timp, ca parte a studiului ereditar PAR și în absența unui istoric familial de PAR, a fost efectuată o analiză a mutațiilor genetice pentru genele tripsinogenului cationic (PRSS1) și inhibitorului tripsinei pancreatice (SPINK1), găsind o mutație în exonul 2 de PRSS1, o constatare neobișnuită fără un corelat clinic clar. Studiul mutației părintești a fost normal (Dr. Volker Keim, Clinica Universității Leipzig, Germania).
Două luni mai târziu, copilul a prezentat un nou episod de PAR constând din dureri abdominale opresive difuze asociate cu vărsături biliare, pentru care a mers la secția de urgență, a fost investigată o creștere a enzimelor pancreatice cu lipază în 3.545 UI/ml și amilază în 3.720 UI/ml și a fost internat în spital. A fost internat hemodinamic stabil, începând hrănirea tubului nasojejunal, bine tolerat. La admitere a fost efectuată o CT abdominală de control care a arătat o creștere a volumului pancreasului, fără semne de necroză și lichid într-o cantitate regulată peripancreatică și perirenală stângă, compatibilă cu Baltasar D. CT abdominal de control cu o îmbunătățire sinceră a semnelor inflamatorii, cu rezoluția colecțiilor și scăderea volumului pancreasului, fără zone sugestive de necroză. A evoluat stabil, cu o scădere a lipazei serice și cu re-hrănire orală progresivă.
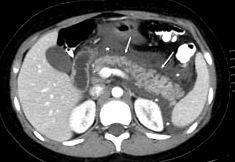
Figura 1. CT al abdomenului, într-o secțiune axială cu utilizarea unui mediu de contrast oral și intravenos, arată o creștere difuză a dimensiunii, neregularitate și alterarea structurii pancreasului (săgeți), asociată cu o creștere a densității de țesut adipos peripancreatic (*) și colecții de lichide (*), fără zone de necroză pancreatică.
Figura 2. MRCP prezintă canalele biliare și canalele pancreatice fără modificări morfologice evidente. HCC: canal hepatic comun; C: canal biliar comun; PC: canalul pancreatic principal (Wirsung); D: duoden.
Discuţie
PAR este o entitate chiar mai rară decât AP și cauzele sale sunt diferite 1 - 3. Etiologia AP la copii este diversă. Trauma abdominală este cea mai frecventă cauză a AP în funcție de diferite serii (20-33%), urmată de etiologie idiopatică (20-35%), calculi biliari și medicamente. Cauzele infecțioase (CMV, coxsackie B, varicela, Salmonella typhi, Campylobacter etc.), cauzele congenitale, cauzele secundare procedurilor invazive ale papilei (ERCP) și cauzele metabolice sunt mai puțin frecvente 4, 5, 7. În pediatrie, este important să se evidențieze fibroza chistică, sindromul Reye și anomaliile structurale congenitale (pancreas divisum) în studiul unui copil cu AP 1 - 3 .
Pancreatita acută recurentă (RAP) este definită ca episoade de pancreatită acută cu rezoluție clinică completă între imagini și cu recuperare completă a parenchimului pancreatic. PAR poate fi împărțit în 5 categorii care ghidează un diagnostic definitiv. Acestea sunt: boala indusă de medicamente, hipertrigliceridemia, bolile oculte ale căilor biliare sau pancreatice, pancreatita familială (ereditară) și idiopatica.
În timp ce multe medicamente pot provoca pancreatită (aproximativ 100), puține s-au dovedit de fapt că provoacă pancreatită la om. Acestea sunt azatioprină și 6-mercaptopurină, sulfonamide, tiazide, furosemidă, estrogeni, tetraciclină intravenoasă, acid valproic și pentamidină. În majoritatea cazurilor, dezvoltarea PA nu este dependentă de doză. Principala complicație a AP în raport cu consumul de droguri este formarea pseudochisturilor pancreatice (PP) 3, 8, 15 .
Hipertrigliceridemia este una dintre cauzele PAR care adesea nu este investigată în mod adecvat. Pacienții cu PAR au niveluri ridicate de trigliceride în sânge, cu niveluri de> 500 mg/dl, care pot chiar să depășească 3.800 mg/dl.
Pe de altă parte, toți pacienții cu RAP trebuie evaluați cu ERCP sau MRCP, în căutarea unor boli ascunse ale căilor biliare și pancreatice, cea mai frecventă cauză fiind prezența calculilor biliari, urmată de pancreas divisum și diskinezie biliară.
Pancreatita familială sau ereditară (PH) se poate prezenta ca orice tip de pancreatită și poate prezenta toate complicațiile pancreatitei alcoolice8. Este o boală autosomală dominantă ale cărei manifestări clinice tipice includ episoade recurente de AP care nu se disting de alte etiologii ale AP și care încep de obicei în copilărie și pot evolua spre pancreatită cronică (CP) și/sau cancer pancreatic. În 60 până la 80% din cazuri există o mutație în gena cripta tripsinogenă (R122H, N29I), cu toate acestea, nu a fost stabilită o relație cauză-efect pentru multe dintre mutațiile care sunt identificate activ 12, 13 .
În cele din urmă, pancreatita idiopatică apare la aproximativ 20-35% dintre pacienții cu PAR, fără o cauză identificabilă; cu toate acestea, mulți dintre acești copii pot avea microlitiază sau mutații necunoscute. 8, 15 .
În ultimii ani, au fost identificați mulți factori genetici de risc pentru CP, prezența mutațiilor în tripsinogen cationic (N29I și R122H) fiind cel mai mare risc. Mutațiile inhibitorului seric de protează (un inhibitor important al tripsinei pancreatice) au fost asociate cu CP idiopatică și CP alcoolică 13, 14 .
În cadrul studiului imagistic, SUA pot fi utile în evaluarea inițială a acestor pacienți, deși poate fi normal în cazurile de AP. Deși poate prezenta o creștere a dimensiunii pancreasului și modificarea structurii sale interne, cea mai bună performanță a sa este în detectarea și monitorizarea colecțiilor lichide, pseudochisturi 3, 6. CT al abdomenului și pelvisului permite o demonstrație anatomică excelentă a pancreasului și poate prezenta o inflamație ușoară a pancreasului chiar și fără creșterea enzimelor pancreatice. Deoarece, în unele cazuri, RAP este secundar calculilor biliari oculti, se sugerează efectuarea unei examinări a bilei sau a fluidului duodenal în căutarea microcristalelor sau efectuarea unui studiu imagistic în mod repetat, așa cum sa întâmplat cu pacientul nostru.
Criteriile clinice ale lui Ranson și criteriile de imagistică ale lui Baltasar au fost utilizate în evaluarea prognostică a AP, care sunt validate la adulți. În prezent, a fost adăugat așa-numitul indice de severitate Baltasar, care evaluează împreună gradul de inflamație pancreatică și procentul de necroză glandulară, care au fost evaluate și în Chile 9 .
Cea mai importantă complicație a PAR este șocul care apare în primele 24 până la 48 de ore de la debutul afecțiunii și poate duce la moartea pacientului dacă nu se efectuează un tratament precoce și adecvat. Printre alte complicații se remarcă hipocalcemia, icterul, complicațiile pulmonare (atelectazie, revărsat pleural), insuficiența renală, sepsisul, necroza pancreasului, abcesele și PP 1, 6. .
În istoria naturală a PAR idiopatic, se poate dezvolta pancreatită cronică sau cancer pancreatic, care este a patra cauză de deces în Statele Unite la adulți. Aproximativ 90% dintre pacienți sunt diagnosticați în etape nerezecabile, ceea ce evidențiază importanța studiului etiologic al PAR, inclusiv un studiu genetic precoce.
Pancreatita cronică se caracterizează prin prezența calcificărilor, dilatarea canalelor pancreatice sau histologia tipică a CP. Progresia unui CP determinat genetic are loc în 3 faze: o fază inițială, cu simptome care necesită spitalizare; o fază intermediară cu un risc crescut de a dezvolta calcificări pancreatice, dilatație ductală și necesitatea unei intervenții chirurgicale; și o fază târzie cu dezvoltarea diabetului. Acest lucru este important pentru a-l putea diferenția de progresia CP alcoolică, care are o progresie mai rapidă și este principala cauză a CP la adulți 16 .
Tratamentul PA va depinde de severitatea acesteia. În TA ușoară, sunt necesare doar odihnă, post, hidratare intravenoasă, înlocuirea electroliților și analgezie. Aspirarea printr-un tub nazogastric poate fi utilă în reducerea simptomelor, dar nu scurtează timpul bolii. În PA moderată și severă, este necesară gestionarea UCI pentru resuscitare adecvată în caz de șoc hipovolemic, insuficiență renală și insuficiență respiratorie. .
Pacienții cu AP prezintă un metabolism similar cu cei cu sepsis, deoarece există o stare hipermetabolică care va necesita un sprijin nutrițional adecvat. Recomandarea actuală la pacienții care nu au primit alimente mai mult de 7 până la 10 zile și care nu prezintă ileus este de a începe nutriția enterală printr-un tub nazojejunal (distal față de unghiul lui Treitz), care trebuie controlat periodic radiologic pentru a detecta o posibilă migrație. Nutriția parenterală totală este rezervată pacienților care necesită aport nutrițional agresiv, la care nu se realizează un acces enteral adecvat sau care progresează nefavorabil cu nutriția enterală. Hrănirea orală va fi reluată în conformitate cu următoarele criterii: absența durerii abdominale, reducerea nivelurilor serice de amilază și lipază la niveluri apropiate de normal, absența complicațiilor și rezolvarea ileonului cu revenirea zgomotelor aer-lichide 2 .
Referințe
Lucrare primită la 5 ianuarie 2007, acceptată spre publicare la 29 martie 2007.
Tot conținutul acestei reviste, cu excepția cazului în care este identificat, se află sub o licență Creative Commons
Primarul Eduardo Castillo Velasco 1838
Ñuñoa, Santiago
Caseta 593-11
- Prezentarea cazului de pancreatită acută recurentă
- Pancreatită acută severă și precoce datorată liraglutidei
- Pancreatita acută Revista de Gastroenterología de México
- Plicație gastrică laparoscopică, o nouă procedură bariatrică subiectul unui caz clinic
- Osteomielita cronică supurativă în raportul maxilar al unui caz clinic